制备亚微米三氧化钨超细粉末2/2
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月25日 星期五 12:53
- 点击数:729
这里再作一些补充说明:
(1)其实,三氧化钨还原为钨粉并不是一步到位的,就拿一个三氧化钨晶体来说,它还原时首先被还原为WO2,然后WO2.9的表面进一步被还原为WO2.72,此时晶体内部还是WO2.9,继续还原时,再变成WO2,最后才被完全还原为钨粉。所以说,三氧化钨还原时,其表面和内部的还原进程并不是同步的。晶体内部的三氧化钨还原得到的H2O必需通过外层已还原的钨扩散到晶体外部,在这种缓慢的扩散过程中极易使晶体产生断裂,在更高倍的电镜照片上就可以看到这些裂纹。
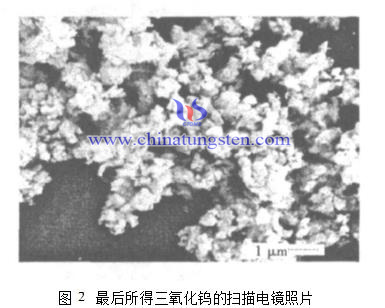
(2)还原后的钨粉要再次氧化时,必须先吸附一定的氧气然后与之反应。可以想象,晶体表面的钨粉很容易吸附氧气,要氧化很简单,但是晶体内部的钨粉氧化,就必须等氧原子扩散到晶体内部之后,或者通过钨粉表面的裂缝吸附大量的氧原子之后才能与之反应。这个过程很缓慢。当晶体内部的钨粉被氧化为三氧化钨后,其体积必然比原来的钨粉的要大,这样就有可能把较大体积的晶体撑裂,整个晶粒就比原来的晶粒要小了。
(3)关于晶粒团聚。颗粒越小的晶体活性越高,这样,距离较近的晶体就更容易相互吸引,更易形成团聚。最后一步得到的三氧化钨颗粒已经非常细小,能够制得亚微米尺度的三氧化钨粉末,达到了预期的实验效果。
氧化还原的过程中,三氧化钨和钨粉的粒度分布不均匀。氧化后生成的三氧化钨有团聚现象,而还原后生成的钨粉团聚现象不明显,钨粉表面有裂纹。很显然,用氧化还原的方法来制备亚微米三氧化钨简单实用。
| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


制备亚微米三氧化钨超细粉末1/2
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月25日 星期五 12:45
- 点击数:766
由于细晶粒硬质合金的种种优异性能,亚微米粉末(平均颗粒尺寸<1m)的需求近年来呈快速上升的趋势。今天,已经能够工业化生产超细钨粉(平均颗粒尺寸<0.5m)。生产超细钨粉对氧化物原料提出了越来越高的要求,特别是在原料的纯度和均匀性方面。
制备超细三氧化钨粉末的方法有很多种,以下采用的是多次氧化还原的方法。实验步骤:
(1)在空气中煅烧APT,温度500℃。
(2)在氢气中还原煅烧后所得的三氧化钨,温度850℃,保温25min。
(3)在空气中氧化第一次还原后所得的钨粉,温度500℃,保温20min。
(4)在氢气中还原第一次氧化后的三氧化钨,温度850℃,保温25min。
(5)在空气中氧化第二次还原后所得的钨粉,温度500℃,保温20min。
(6)第二次氧化后所得三氧化钨和第二次还原所得钨粉在蒸馏水中分散后作激光粒度分析。
(7)用分析纯酒精分散氧化钨和钨粉后作电子探针扫描。

图一各步实验所得产物之粒度分布图
实验结果分析:
ATP经煅烧后所得的三氧化钨,大部分呈松针状聚集在一起。在氢气气氛下还原时,团聚的三氧化钨表面首先被还原,使表面密度变小,因为三氧化钨被还原时由于脱氧而生成钨粉,体积明显变小。也就是说,团聚表面变得蓬松。这样,团聚内部的三氧化钨还原时会把表面的钨粉撑裂,使团聚表面出现很多微裂纹。也有的团聚粒径较大,表面能较小,裂纹更深,直接导致团聚裂开,分裂成几块更小的团聚。所以,经过还原以后的钨粉形状比较规则。这样,当生成的钨粉被氧化时,团聚表面的钨粉直接氧化成三氧化钨。但是,团聚内部的钨粉要被氧化,氧原子就要通过团聚表面的裂缝进入内部与钨粉相结合,这足以使裂纹扩大以致使团聚裂开。这就是虽然钨粉结合了氧原子,但颗粒粒径还是会变小的原因。关于生成的三氧化钨有团聚现象的原因,可以认为是因为氧化反应结合氧原子,使本来就靠得比较近的钨粉之间填充了氧,从而形成团聚。 还原的氧化钨再次氧化以后,三氧化钨颗粒粒径明显变小,其原因仍在于还原时脱氧和钨粉产生裂缝。
| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


重结晶法制备高纯度仲钨酸铵
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月25日 星期五 09:52
- 点击数:1099
 深度加工钨产品的质量直接受仲钨酸铵(APT)质量的影响,生产掺杂钨丝和钨合金丝所用的仲钨酸铵结晶粉末,每种杂质含量不应超过2*10-5,因此,要制得高纯度的仲钨酸铵,以满足工业生产的需求。现在常用的方法有重结晶法、电解法等。本文主要讲述重结晶法制备高纯度仲钨酸铵。
深度加工钨产品的质量直接受仲钨酸铵(APT)质量的影响,生产掺杂钨丝和钨合金丝所用的仲钨酸铵结晶粉末,每种杂质含量不应超过2*10-5,因此,要制得高纯度的仲钨酸铵,以满足工业生产的需求。现在常用的方法有重结晶法、电解法等。本文主要讲述重结晶法制备高纯度仲钨酸铵。| 仲钨酸按供应商:中钨在线科技有限公司 | 产品详情: ammonium-paratungstate.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


改进后的Na2S从钨酸钠溶液中除钼
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 18:32
- 点击数:1288
| 钨酸钠供应商:中钨在线科技有限公司 | 产品详情: http://www.sodium-tungstate.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


选择性沉淀法从钨酸钠溶液中除钼
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 18:30
- 点击数:933
| 钨酸钠供应商:中钨在线科技有限公司 | 产品详情: http://www.sodium-tungstate.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


仲钨酸铵循环氧化还原法制备亚微米球形钨粉
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 17:52
- 点击数:1021

特纯仲钨酸铵循环氧化还原法制备亚微米球形钨粉的原理是,将仲钨酸铵煅烧得到紫钨,再对紫钨进行还原,得到钨粉,对制得的钨粉进行循环2次氧化和3次还原。工艺生产过程如下:
循环氧化还原法因其独有的受污染少、粒度分布范围窄、工艺路线简捷易行、工艺参数易于控制、设备简单和适合工业化大批量生产等优点在众多方法中脱颖而出,并且,制得的亚微米钨粉颗粒呈球形,有利于钨粉在压坯烧结过程均匀化收缩,实现良好的尺寸控制。
| 偏钨酸铵供应商:中钨在线科技有限公司 | 产品详情: ammonium-metatungstate.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


铁系金属氧化物掺杂对三氧化钨陶瓷热电性能影响5/5
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 17:35
- 点击数:834
| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


铁系金属氧化物掺杂对三氧化钨陶瓷热电性能影响4/5
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 17:33
- 点击数:820
| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


铁系金属氧化物掺杂对三氧化钨陶瓷热电性能影响3/5
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 17:31
- 点击数:829
| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |


铁系金属氧化物掺杂对三氧化钨陶瓷热电性能影响2/5
- 详细资料
- 分类:钨业知识
- 发布于 2015年12月24日 星期四 17:29
- 点击数:840

| 氧化钨供应商:中钨在线科技有限公司 | 产品详情: http://www.tungsten-oxide.com |
| 电话:0592-5129696 传真:5129797 | 电子邮件:sales@chinatungsten.com |
| 钨钼文库:http://i.chinatungsten.com | 钨钼图片: http://image.chinatungsten.com |
| 钨新闻3G版:http://3g.chinatungsten.com | 钼业新闻: http://news.molybdenum.com.cn |