鎢氧化物的晶體結構
- 詳細內容
- 分類:鎢新聞
- 發佈於:2023-02-03, 週五 21:56
- 作者 Caodan
- 點擊數:588
三氧化鎢(WO3)是目前被最廣泛使用的鎢氧化物,完美的WO3是一種ReO3類型的立方體晶體結構材料,其中八面體的WO6通過分角而相互連接。在WO6八面體中,W原子位於中心,其餘六個O原子形成八面體框架。隨著溫度和壓力的變化,WO6八面體會以一定的角度傾斜和旋轉,導致形成幾種不同的相:四邊形相、正方體相、單斜體相、三斜體相和立方體相。
在WO3內部,八面體之間有一些位點和隧道,因此小直徑的原子,如H+、Li+和K+可以轉移到WO3中並被儲存。還有另一種WO3的相,即六方相,可以從水合鎢氧化物的水合過程中得到。在WO6八面體堆積後,沿著c軸形成了三棱柱和六棱柱隧道。這些隧道有利於離子和電子的快速轉移,所以六方鎢氧化物的電化學活性要比其他相的WO3好。最常見的三氧化鎢相是單斜相(m-WO3),六方相(h-WO3)。
在天然存在的WO3中,缺氧是非常常見的,導致存在亞化學計量的鎢氧化物,WO3-x(0 < x < 1),其中W的價位可能是+3、+4或+5。其中,W18O49、W20O58和W24O68是最常見的,它們內部的缺氧可以促進其導電性。這一特性使WO3成為n型半導體,其導電性可以通過控制其中的O空位量來調整。
由液體相關方法製成的鎢氧化物通常是熱處理前的水合鎢氧化物,即WO3-xH2O,主要包括WO3-0.33H2O、WO3-0.5H2O、WO3-H2O和WO3-2H2O。WO3-xH2O的結構主要由x的值決定。例如,WO3-H2O的結構是H2O位於WO6八面體的層間空隙中,而WO3-2H2O的晶體結構是除了WO3-H2O中的同類H2O分子外,另一類H2O分子直接與八面體底部或頂部的鎢原子連接。這種結構有利於離子和電子,特別是質子通過它們內部的氫鍵網路輕鬆地傳輸。通常情況下,水合氧化鎢比純氧化鎢有更好的導電性,轉化為增強的電化學性能。
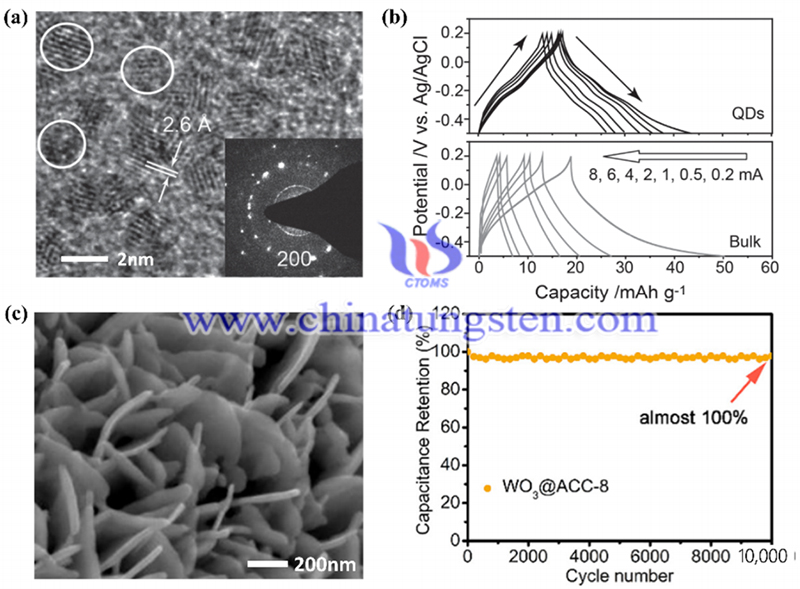
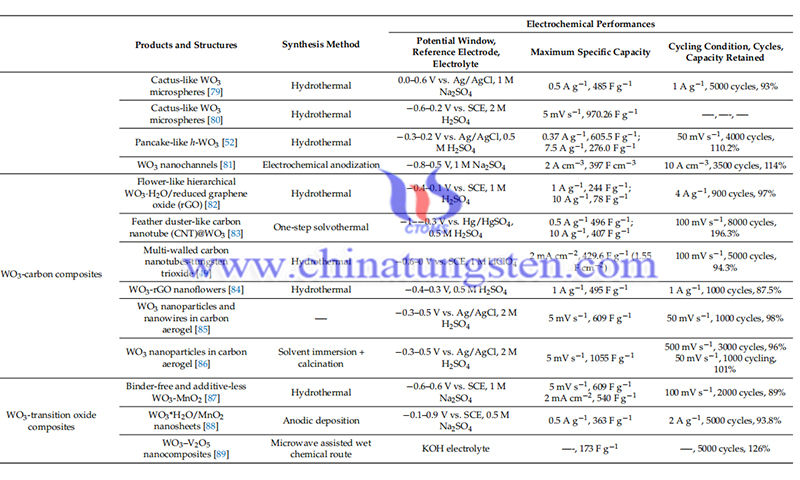
參考文獻:Han W, Shi Q, Hu R. Advances in electrochemical energy devices constructed with tungsten oxide-based nanomaterials[J].《納米材料》, 2021, 11(3): 692.
| 鎢產品供應商:中鎢在線科技有限公司 | 產品詳情: http://cn.chinatungsten.com |
| 電話:0592-5129696 傳真:5129797 | 電子郵件:sales@chinatungsten.com |
| 鎢鉬文庫:http://i.chinatungsten.com | 鎢鉬圖片: http://image.chinatungsten.com |
| 鎢業協會:http://www.ctia.com.cn | 鉬業新聞: http://news.molybdenum.com.cn |





 sales@chinatungsten.com
sales@chinatungsten.com